喘息などのアレルギー疾患が悪化するメカニズムを解明-脂肪分解経路を標的とした新たなアレルギー治療薬の開発に向けて-
千葉大学大学院医学研究院 平原 潔教授と横浜市立大学大学院医学研究科 金子 猛教授、柳生 洋行助教(研究当時:千葉大学大学院医学薬学府 特別研究学生)らの研究グループは、アレルギー性炎症を悪化させる「病原性Th2(ティーエイチツー)細胞」注1)が、免疫細胞が持つ「脂肪滴を分解して再利用する仕組み」によって誘導されることを明らかにしました。今後、脂肪分解経路を標的とした新たなアレルギー疾患の治療法の開発が期待されます。
本研究成果は、2025年10月24日に、国際科学誌Science Immunology に公開されました。
本研究成果のポイント
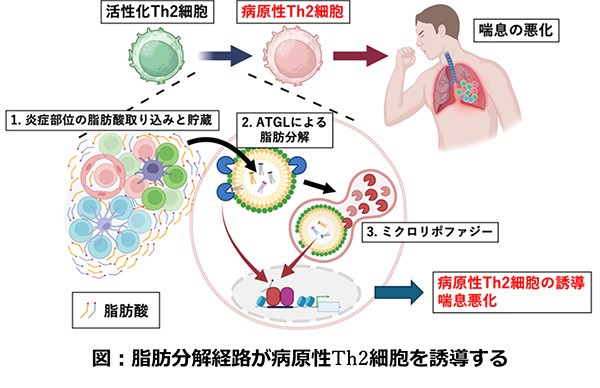
今回の研究の結果、抗原刺激で活性化したTh2細胞が、炎症組織で増加する特定の脂肪酸を「脂肪滴」として細胞内に燃料として蓄えること、その「脂肪滴」を脂肪分解酵素やオートファジー注2)機構によって少しずつ分解(燃焼)することで、病原性Th2細胞が誘導されることを突き止めました。
- 喘息モデルマウスの炎症部位では、オレイン酸などの「脂肪酸」が顕著に増加していた(図中1)
- その脂肪酸を、活性化したTh2細胞が取り込んで「脂肪滴」に一時的に蓄積し、脂肪分解酵素ATGL注3)(図中2)や「ミクロリポファジー」注4)と呼ばれる特殊なオートファジー機構(図中3)によって脂肪滴を分解することで、病原性Th2細胞が誘導された。
- 脂肪分解酵素ATGLを欠損させたマウスでは、ミクロリポファジーの抑制、病原性Th2細胞の減少とともに、喘息の主症状である好酸球性気道炎症の改善も確認した。
- 好酸球性副鼻腔炎患者においても脂肪分解経路を介した病原性Th2細胞誘導機構が同様に働いていることを確認し、難治性の病態との関連を示した。
【用語解説】
注1)病原性Th2細胞:
Th2細胞は、免疫の司令塔となるヘルパーT細胞の一種で、特に寄生虫に対する感染から体を守る。一方で、アレルゲン(ダニや花粉など)に対しても反応し、炎症を引き起こす物質(サイトカイン)を分泌する。このTh2細胞の中でも一部の集団が病原性Th2細胞となる。病原性Th2細胞は、アレルゲンを記憶して炎症組織に長くとどまり、再びアレルゲンを感知すると多量のサイトカインを分泌し、通常のTh2細胞よりも強い炎症を引き起こす。喘息などのアレルギー疾患の慢性化や難治化に関与する。
注2)オートファジー:
細胞内部の異常なタンパク質や不要になったタンパク質、細胞小器官をリソソーム(細胞内の分解装置)で分解・再利用する仕組みで、「自食作用」とも呼ばれる。細胞を正常な状態に保つための重要な維持管理機能。
注3)ATGL:
脂肪滴の内に貯蔵された中性脂肪(トリグリセリド)を分解する酵素で、細胞が脂肪をエネルギー源として利用する際に中心的な役割を果たす。
注4)ミクロリポファジー:
脂肪滴を分解する特殊なオートファジーで、細胞内の分解装置であるリソソームが脂肪滴を直接取り込んで分解する現象を指す。
研究内容の詳細
喘息などのアレルギー疾患が悪化するメカニズムを解明-脂肪分解経路を標的とした新たなアレルギー治療薬の開発に向けて-(PDF:1MB)
本学の共同研究者
大学院医歯学総合研究科 青木亜美 助教
論文情報
【掲載誌】Science Immunology
【論文タイトル】Lipolysis–microlipophagy cascade regulated by adipose triglyceride lipase drives pathogenic adaptive type 2 immunity
【著者】Hiroyuki Yagyu, Masahiro Kiuchi, Atsushi Sasaki, Eisuke Itakura, Kota Kokubo, Chiaki Iwamura, Atsushi Onodera, Ami Aoki, Takahisa Hishiya, Kaori Tsuji, Takuto Hiramoto, Rie Shinmi, Yuri Sonobe, Takahiro Arano, Kanae Ohishi, Shigenori Baba, Junya Kurita, Tomohisa Iinuma, Syuji Yonekura, Yu Hara, Motoko Yagi Kimura, Shinichiro Motohashi, Damon J Tumes, Toyoyuki Hanazawa, Takeshi Kaneko, Toshinori Nakayama, Kiyoshi Hirahara
【doi】10.1126/sciimmunol.adp0849
本件に関するお問い合わせ先
広報事務室
E-mail pr-office@adm.niigata-u.ac.jp